作者:北京积水潭医院核医学科 张毓艺 杨芳
病史及检查目的:
患者男性36岁,主因“双侧大腿骨折术后4年,局部渗液8月余”入院。患者4年前因车祸导致右股骨干开放性骨折,左股骨干、左髌骨、右尺骨鹰嘴等处多发骨折;伤后当日予清创缝合术,1月内先后行右股骨骨折支架外固定、右尺骨鹰嘴骨折切开复位内固定、右股骨骨折拆除外支架改髓内针内固定等。3年前因右股骨干内固定物术后感染行扩创、内固定取出术,术后右大腿无明显疼痛,活动尚可;8个月前出现发热伴右大腿红肿疼痛、流黄脓伴渗液及出血,予抗感染等对症处理后,局部症状缓解不明显。查体:右大腿皮肤窦道,局部少许黄白色渗液及多处手术疤痕。实验室检查:WBC 10.55×109/L(参考值3.5-9.5×109/L);ESR:41mm/h (参考值:0-15mm/h);CRP:29.0mg/L(参考值<8mg/L)。为明确感染活动性及其范围行双大腿部位18F-FDG PET/CT显像。
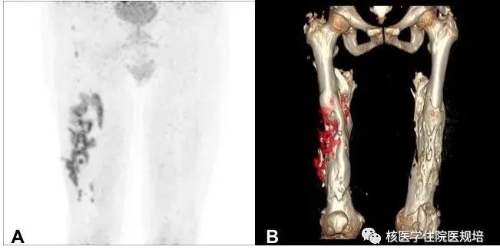
图1 A:双大腿PET MIP图;B:AW VR 3D重建图
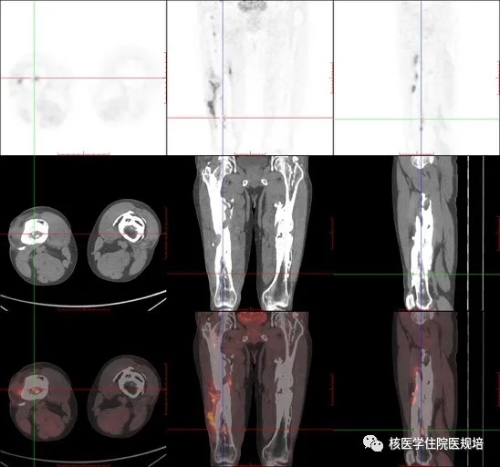
图2 右大腿软组织感染,双侧股骨骨折术后愈合不良
图3 右股骨下段髓腔内多发FDG代谢增高灶
检查所见:
右股骨骨干增粗变形,骨质密度弥漫增高,中段骨皮质不连续;右股骨上段及下段骨髓腔内可见多发FDG摄取增高灶(SUVmax分布在5.0~5.8),CT示髓腔内密度增高;右大腿中下段软组织内见弥漫性FDG摄取增高(SUVmax:11.9),累及长度约23cm,病灶外下方见窦道形成,并与骨组织相通,深约3.8cm,另软组织内见多发不规则钙化及骨化。
左股骨中段骨皮质不连续,髓腔内密度弥漫增高,左大腿软组织内见分层状不规则钙化及骨化密度影,FDG摄取未见明显异常。
检查意见:
1、右股骨骨折术后愈合不良,右大腿多发FDG代谢增高灶,考虑为感染性病灶,病变累及骨髓腔及周围软组织内。
2、左股骨骨折术后愈合不良,未见明显活动性感染征象。
3、双大腿软组织骨化性肌炎。
最终临床诊断:
患者随后行“右股骨干骨髓炎扩创术、抗生素人工骨置入术”,术中见大腿外侧软组织内大量增生肉芽组织及骨水泥链珠,彻底扩创、切除坏死组织,标本送细菌培养及药敏。细菌培养结果示金黄色葡萄球菌阳性,证实活动性感染存在。
病例相关知识及解析:
骨折术后感染是创伤骨科手术后最常见且严重的并发症。开放性骨折术后、骨折切开复位或其他骨关节手术后出现感染会导致创伤后骨髓炎的发生。感染部位都发生在骨折端附近,病程可分为急性或慢性。导致内固定物术后感染最常见的致病菌为金黄色葡萄球菌[1],如本例患者,最终细菌培养即为金黄色葡萄球菌。
明确内固定物术后感染的诊断对于临床决策至关重要,且感染灶的定位直接影响临床治疗方式的选择。对于此类患者,临床需结合患者症状、实验室检查、组织病理学、细菌生物学及影像学检查做出综合诊断。其中,患者症状并无特异性,CRP、ESR升高有一定的提示意义但其证据等级较低,仅作为参考。传统的形态学影像检查如X线、CT和MR为临床一线检查,但这些检查手段均存在各自的局限性。X线平片诊断骨骼肌肉系统感染的灵敏度和特异度较低,分别为50-75%、75-83%[2],且骨髓炎发病2周内X线常无异常发现,因此会延误骨髓炎患者的诊断和治疗。MR检查的灵敏性较高,在骨髓炎发病2天内可有阳性表现,如最早期的骨髓水肿、周围软组织水肿和骨膜反应,但内置的金属固定物会在MR图像上造成严重伪影,且难以观察骨质改变。以揭示功能性改变见长的核医学检查可作为常规影像检查的重要补充。应用于骨髓炎的核医学检查手段包括骨显像、三时相显像、标记白细胞联合骨髓显像、67Ga/68Ga标记炎症显像、IgG显像、以及FDG PET/CT显像等[2]。三时相骨显像对于诊断骨髓炎具有高度敏感性,平台第130号病例有相关内容报道,但其特异性较低。文献报道,其对单纯骨髓炎患者诊断准确性尚可,而对于创伤后或其他手术后患者的诊断特异性仅为35%[3],因此存在一定的假阳性率而易造成误诊。
18F-FDG作为目前PET临床应用最广泛的放射性药物,不仅在恶性肿瘤病灶中大量聚集,同时也可以在炎症组织内葡萄糖代谢增强的活化炎性细胞(以中性粒细胞、巨噬细胞为主)中聚集,而使活动性炎症或感染病灶显影。其病理生理机制为:炎症早期血管通透性增加,软组织血流灌注增多,导致更多的FDG在感染部位聚集。随后炎性细胞通过趋化作用聚集到炎性病灶,通过细胞因子刺激、葡萄糖转运蛋白(GLUT1、3)表达上调、己糖激酶活性增强等复杂机制共同作用下,使得炎性细胞的葡萄糖代谢活性增强[4]。有研究表明,无论炎症处于急性期或慢性期,FDG摄取均与炎性细胞数量呈线性正相关[5]。PET/CT显像集功能与解剖成像于一体,利用FDG PET在代谢水平的高度准确性,以及CT对骨质及软组织形态改变的检出,可对骨髓炎的活动性及范围作出精准的诊断。文献显示,PET/CT对急性或慢性骨及软组织感染的灵敏性可高达95%以上,特异性在75-99%[6]。2019年,由四个欧洲学会联合发表的成人外周骨感染诊断指南中[7],18F-FDG PET/CT作为2级证据水平,被推荐常规应用于高度怀疑骨折术后感染的患者。
本例患者创伤史较长,同机CT表现为双侧股骨增粗变形、骨质密度增高,整体符合慢性骨髓炎影像特点;同时结合PET表现,右大腿骨折断端周围软组织内及骨髓腔呈现明显高代谢,提示了慢性骨髓炎活动性感染部位。尽管左侧大腿肌肉组织内亦可见不规则骨样组织(即骨化性肌炎表现),但无明显代谢活性增高区,单纯表现为骨折后的慢性骨质增生修复,从而排除了活动性感染。最终手术所见及菌培证实了PET/CT检查的诊断结果。
小结:
对于创伤后可疑骨髓炎患者,18F-FDG PET/CT可以提示活动性感染存在与否、术前协助确定感染范围并辅助评估抗感染治疗效果。与传统影像学检查(X线、CT、MR)相比,能够为创伤后骨髓炎患者提供一种基于代谢改变的、更为精准的影像诊断方法,具有较好的临床应用前景。
参考文献:
1. Morgenstern M, Kühl R, Eckardt H, et al. Diagnostic challenges and future perspectives in fracture-related infection. Injury. 2018, 49 Suppl 1: S83-S90.
2. Palestro CJ. Radionuclide Imaging of Musculoskeletal Infection: A Review. J Nucl Med. 2016, 57(9): 1406-1412.
3. van der Bruggen W, Bleeker-Rovers CP, Boerman OC, et al. PET and SPECT in osteomyelitis and prosthetic bone and joint infections: a systematic review. Semin Nucl Med. 2010, 40(1): 3-15.
4. Vaidyanathan S, Patel CN, Scarsbrook AF, et al. FDG PET/CT in infection and inflammation--current and emerging clinical applications. Clin Radiol. 2015, 70(7): 787-800.
5. Irmler IM, Opfermann T, Gebhardt P, et al. In vivo molecular imaging of experimental joint inflammation by combined (18)F-FDG positron emission tomography and computed tomography. Arthritis Res Ther. 2010, 12(6): R203.
6. Love C, Palestro CJ. Nuclear medicine imaging of bone infections. Clin Radiol. 2016, 71(7): 632-646.
7. Glaudemans AW, Jutte PC, Cataldo MA, et al. Consensus document for the diagnosis of peripheral bone infection in adults: a joint paper by the EANM, EBJIS, and ESR (with ESCMID endorsement). Eur J Nucl Med Mol Imaging. 2019, 46(4): 957-970.