作者:北京大学人民医院核医学科 赵赟赟 王茜
病史及检查目的:
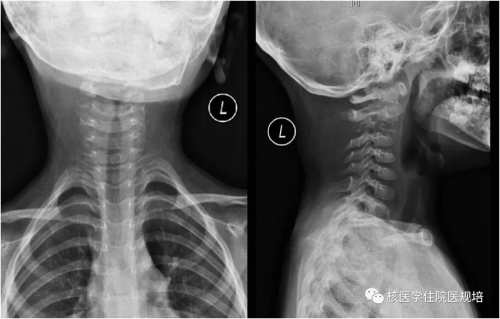
患儿为3岁女性,主因“发现颈椎肿物3个月”就诊。患儿3个月前因颈部疼痛就诊,行颈椎正侧位X光片检查,结果示C3椎体明显变扁呈“钱币”样,棘突可见骨质破坏(图1)。查体:C3椎体附近触及一大小约为3.0×4.0cm肿物,有压痛,活动性差,浅表淋巴结未触及。实验室检查无特殊发现。胸部CT及腹部超声未见明显异常。为进一步评估骨病变累及范围,行99mTc-MDP全身骨显像(图2)。
图1 颈椎正侧位X线片
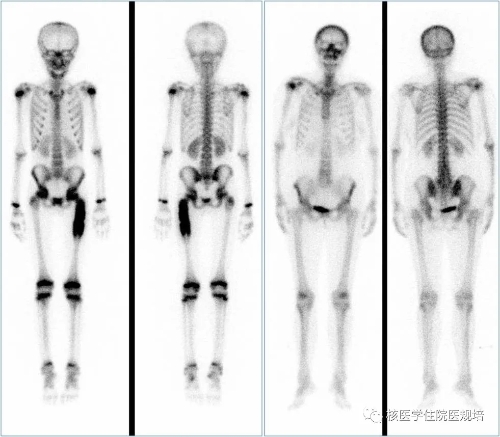
图2 全身骨显像
检查所见:
静脉注射99mTc-MDP 4小时后行全身前、后位平面显像。影像所见:全身骨骼显像清晰,脊柱放射性分布不均匀,上位颈椎相当于C3椎体水平可见条片状不均匀放射性浓聚灶,其余诸骨未见明显异常放射性分布。
检查意见:
上位颈椎相当于C3椎体水平片状轻度示踪剂摄取增高,符合langerhans细胞组织细胞增生症表现,余骨未见明确受累征象。
最终临床诊断及随访:
患者随后行C3椎体病变穿刺活检,病理结果示:纤维组织中可见灶片状嗜酸性粒细胞浸润,其间可见小灶状组织细胞样细胞及散在多核巨细胞成分,个别细胞可见核沟,免疫组化染色结果:CD1a(+),CD68(-),S-100(+),符合Langerhans细胞组织细胞增生症。
患儿术后未再行其他治疗,3个月后其家长无意中触及患儿头顶部质硬包块,伴触痛,实验室检查发现WBC13.12×109/L(参考值3.5-9.5×109/L),LY%:55.8%(参考值20%-50%),PLT:403×109/L(参考值125-350×109/L),LDH:404U/L(参考值109-245U/L),CRP:33mg/L(参考值<8mg/L),ESR:54mm/h(参考值<20mm/h)。为进一步评估病变累及范围,行FDG PET/CT检查(图3)。
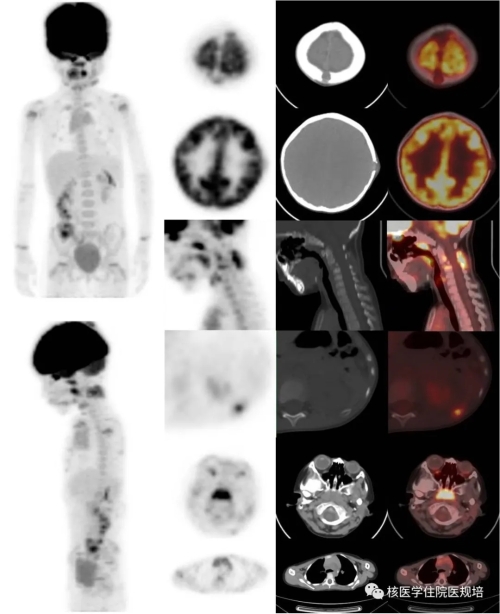
图3 FDG PET/CT影像
检查所见:
顶骨正中、左侧颞骨见多发骨破坏区,伴软组织肿块形成,其内可见纽扣样死骨,相应区域均呈FDG摄取增高表现(SUVmax分布于3.4~4.1);C2-4椎体及附件见溶骨性骨破坏及周围软组织肿物影,FDG摄取增高(SUVmax:4.7),其中C3椎体明显压缩变扁,呈“钱币”征;左侧第11后肋可见一条状沿肋骨走形的FDG摄取增高灶(SUVmax:4.5),CT见溶骨性骨质破坏;双侧颈后部皮下见数个扁平状软组织结节影,直径分布于1.0~2.0cm,呈FDG高摄取表现(SUVmax分布于1.0-2.4);双侧颈动脉鞘周围及颌下见多发FDG摄取增高的淋巴结影(SUVmax:2.3),短径分布于0.5~0.8cm,部分形态较圆;鼻咽顶、后壁及双侧扁桃体区可见片状FDG摄取(SUVmax:5.2),相应部位CT见局部软组织增厚。胸腺形态饱满并可见弥漫性FDG摄取(SUVmax:2.3),CT未见异常密度影;扫描范围内其余部位未见明显异常FDG摄取或结构改变。
检查意见:
1.PET/CT显像示多发FDG代谢增高灶均可符合langerhans细胞组织细胞增生症表现,病变累及颅骨、颈椎、颈后皮下软组织、双侧颈部淋巴结
2.鼻咽部、双侧扁桃体和胸腺形态饱满伴FDG代谢增高,考虑生理性摄取可能性大。
病例相关知识及解析:
朗格罕斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)是一种临床少见的以树突细胞在多个器官的单克隆异常增殖及聚集为主要表现的疾病,可发生于任何年龄,但主要见于儿童,0~15岁的发病率为每年5.4/100万,发病高峰为1~3岁,男性略多。病变最常累及骨骼,同时还可累及皮肤、肺、肝、脾、垂体、淋巴结和造血系统等。患者症状复杂多样,实验室检查缺乏特征性,确诊依赖在病理和免疫组化检查中发现具有特征性的朗格汉斯细胞及 Langerin、CD1a、S-100染色阳性,或者电子显微镜下观察到细胞内Birbeck颗粒。LCH既往也称组织细胞增多症X,根据其临床特点划分为嗜酸性肉芽肿(eosiphilic granuloma,EG)、韩-薛-柯病(Hand-Schuller-Christian Disease,HSCD)和勒-雪病(Litterer-Siwe Disease,LSD)三种类型;进一步研究发现,显微镜下组织细胞增多症X的主要细胞成分为langerhans细胞,故更名为langerhans细胞组织细胞增多症。
临床上LCH最常见的累及部位是骨骼,其中尤以中轴骨和长骨为著,患者可出现局部疼痛,或可触及有轻压痛的隆起性肿块。在组织病理学上,根据病程发展分为朗格汉斯细胞集聚和增生期、肉芽肿期和退缩修复期三个阶段,在X线和CT上出现相应的骨质吸收、溶骨性骨质破坏伴软组织肿物形成和骨质增生硬化性改变,但在不同部位、不同时期的影像表现不尽相同:1)颅骨病变以颅盖骨多见,表现单个或多个穿凿样、溶骨性骨质破坏,呈圆形或卵圆形,可跨越颅缝,局部可形成软组织肿块,病变可相互融合、重叠,内可见残存骨碎片呈“纽扣征”,修复期病变边缘可见硬化。2)脊柱病变以胸椎多见,表现椎体溶骨性破坏并塌陷,侧位观呈“钱币”样扁平椎,临近椎间盘完整,椎间隙增宽。3)骨盆病变以髂骨翼和髋臼上缘多见,表现不规则囊状溶骨性破坏,边缘硬化、锐利,内见死骨。4)肋骨病变以中后段多见,表现囊状或多囊状骨质破坏,可形成胸壁软组织肿块。5)长骨受累以股骨多见,骨破坏多位于骨干和干骺端,不跨越骺板,可穿破骨皮质形成软组织肿块并见层状骨膜反应。在全身骨显像中,病变早期由于langerhans细胞增生形成肉芽肿而替代骨组织,可显示局部示踪剂摄取减低或缺损,而病变后期由于组织修复,病灶周围纤维组织发生骨化,可出现局部示踪剂摄取增高表现,这在长骨受累时尤其明显,呈条索状浓聚灶或范围较小的局灶性浓聚[1](图4),但溶骨性小病灶或位于胸骨、颈椎、髂骨和肩胛骨等早期病变较难发现[2],必要时应进行SPECT/CT显像。
图4 LCH患者的骨显像图像
对于LCH患者来说,病变累及范围不同,其治疗及预后存在差异。国际组织细胞协会将LCH分为单系统LCH和多系统LCH,前者可进一步分为单系统单部位型和单系统多部位型;后者又根据有无危险脏器(肝、脾、肺和造血系统)受累分为危险脏器受累的多系统LCH和危险脏器未受累的多系统LCH。通常单系统LCH预后良好,绝大多数只需要局部治疗或观察,而多系统 LCH ,特别是伴有危险脏器受累者,预后差,目前尚无统一治疗方案,临床试验结果显示长春新碱联合甲泼尼龙可作为多系统LCH患者一线治疗[3],异基因造血干细胞移植和靶向药物治疗也可使患者获益。本例患儿初次入院仅表现C3椎体单一病灶,显示出该病最易累及骨骼的特点,同时根据骨显像检查结果,提示病灶可能处于较早期阶段(溶骨性改变为主)。然而,3个月后患儿又出现了颅顶包块,行FDG PET/CT检查后不仅显示出颈椎、颅骨的多发病灶,同时还显示了颈后软组织和颈部淋巴结多器官系统受累表现。该患儿最终诊断为危险脏器未受累的多系统型LCH,给予长春新碱静脉化疗及甲泼尼龙片口服,头部肿块局部注射地塞米松治疗后头部肿块较前缩小。
FDG PET/CT显像中LCH的病变部位均表现对FDG的高摄取,是因为病变组织中富含炎性细胞(中性粒细胞和多核巨细胞等),其细胞内葡萄糖转运体和己糖激酶活性的升高及葡萄糖代谢的升高导致过多的FDG被摄入细胞内。通过一次性大视野成像,不仅能帮助检出隐匿部位或骨破坏不明显的骨骼病灶,同时可检出骨骼以外器官组织内的病灶,这说明FDG/CT对多系统受累情况的观察具有其他影像技术不可替代的作用,可为临床分型和选择治疗方案提供更准确的信息。此外,通过观察治疗前后病灶处FDG摄取程度的差异,还能为临床疗效评估及预后评价提供依据[4]。
参考文献:
1.邵虹, 施美华, 王静蕾,等. 骨显像在儿童郎格尔汉斯细胞组织细胞增生症诊断及随访中的价值. 中华核医学杂志, 2005, 25(1): 52-53.
2.Howarth DM,Mullan BP, Wiseman GA, et al.Bone scintigraphy evaluated in diagnosing and staging Langerhans' cellhistiocytosis and related disorders. J Nucl Med, 1996, 37(9): 1456-1460.
3.Gadner H, Minkov M, Grois N, et al. Therapy prolongation improves outcome in multisystem Langerhans cell histiocytosis.Blood, 2013, 121(25): 5006-5014.
4.Obert J, Vercellino L, Van Der Gucht A, etal. (18)F-fluorodeoxyglucose positron emission tomography-computed tomographyin the management of adult multisystem Langerhans cell histiocytosis. Eur JNucl Med Mol Imaging, 2017, 44(4): 598-610.