作者:首都医科大学附属北京世纪坛医院核医学科 郑朋腾 童冠圣
病史及检查目的:
患者女性,29岁,主因“间断腹泻1年”收入院。患者1年前无明显诱因出现腹泻,为乳白色水样便,7-8次/日,后出现乳糜尿,7个月前行腹腔镜左肾周围淋巴管剥脱术。术后乳糜尿消失,腹泻加重,伴双下肢及腹盆壁肿胀。外院胶囊肠镜:小肠腔内可见外压性隆起病变。实验室检查:白蛋白16.7g/L(参考值35-50g/L),淋巴细胞0.3×109/L(1.1-3.2×109/L),IgG 4.42g/L(7-16 g/L)。为了解有无肠蛋白丢失及明确全身淋巴回流情况分别行肠蛋白丢失显像(图1)及淋巴显像(图2)。
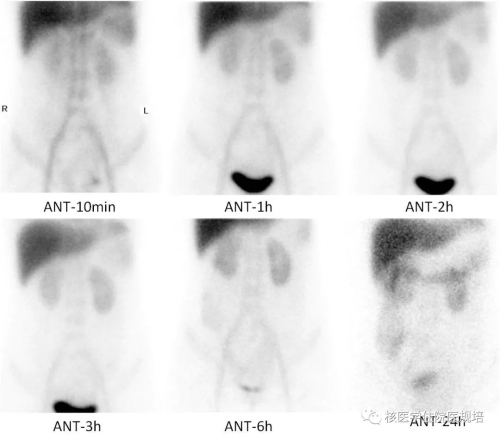
图1 肠蛋白丢失显像
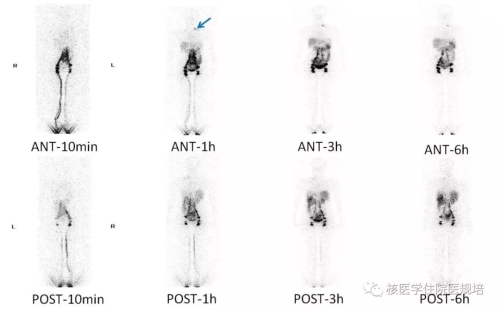
图2淋巴显像
检查所见:
肠蛋白丢失显像:静脉注射99mTc-HSA 20mci后分别于10min、1h、2h、3h、6h、24h采集腹盆腔前位平面图像,结果如下:早期显像可见大血管、心血池、肝脏、双肾显影,随时间延长,上述部位放射性逐渐减淡。6h时见右中下腹部肠管区域开始出现轻度显像剂浓聚,延迟至24小时升、横结肠显影。
淋巴显像:双足第一、二及第四、五趾间皮下注射显像剂(99mTc-DX,5mci×2)后10min、1h、3h和6h分别行全身前、后位平面显像,结果示:双下肢淋巴管、双侧腹股沟、髂、腰淋巴结显影清晰,呈对称性分布,肝脾显影清晰,显像剂回流通畅;10min时腹部开始出现显像剂分布,随时间延长,其分布范围扩大至盆腔;此外,左静脉角持续显影(蓝色箭头所示);腹盆腔左侧可见肠管状显像剂浓聚。
检查意见:
1. 99mTc-HSA显像示肠蛋白丢失
2. 99mTc-DX显像示肠蛋白丢失由肠淋巴管扩张所致,左静脉角持续显影,提示胸导管出口梗阻可能。
临床最终诊断及随访:
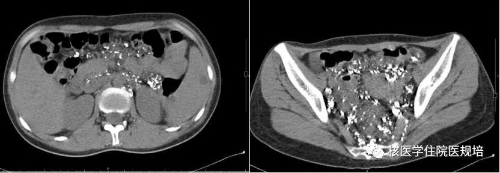
患者随后行直接淋巴管造影:造影剂沿右髂淋巴管、双侧腰干上行,走行紊乱,于L1上缘形成胸导管主干,向上胸导管间断显影,管径增粗,平静呼吸未见造影剂入血征象;可见造影剂向左锁骨下、左颈干、左侧肋间、左肾区域返流,于左肾处形成团块状浓聚影;腹膜后及盆腔可见大量迂曲扩张淋巴管团。淋巴管造影术后立即行腹盆腔CT检查,腹盆腔肠周可见多发软组织密度影,内可见多发点状及结节状造影剂蓄积(图3)。
图3
之后患者行剖腹探查+腹膜后扩张淋巴管切除+肠粘连松解+部分小肠及乙状结肠病损切除,病理示:小肠及乙状结肠肠壁肿物内可见扩张脉管。结合病史,符合淋巴管扩张症。
临床最终诊断胸导管梗阻,肠淋巴管扩张。之后患者行胸导管探查+末端粘连松解术。术后患者症状较前明显好转。
相关知识及病例解析:
肠淋巴管扩张症(intestinal lymphangiectasia,IL)是蛋白丢失性肠病的最常见病因,由Waldmann等于1961年首次报道,以小肠淋巴管回流受阻,肠淋巴管和(或)乳糜管扩张、破裂,淋巴液漏出为主要特征的疾病。IL根据病因不同,可分为原发性和继发性。原发性IL发病机制尚不清楚,目前认为主要是淋巴管先天畸形或发育不良造成了淋巴回流受阻,淋巴管内压力升高,肠淋巴管扩张,多见于儿童及青少年。继发性IL与自身免疫性疾病、肿瘤、感染(结核、丝虫病等)、肝硬化、门静脉高压、缩窄性心包炎、Whipple病、腹部外伤或手术损伤等因素有关,由于淋巴管及周围组织的炎症和狭窄使淋巴循环受压或回流不畅。
肠淋巴管扩张症患者往往起病隐匿,临床症状主要表现为水肿,也可有腹泻、低蛋白血症、淋巴细胞减少、浆膜腔积液等表现。目前国内临床诊断IL主要参照以下标准:1)典型的临床表现;2)外周血淋巴细胞绝对计数减少;3)血浆白蛋白和 IgG 同时降低;4)内镜活检或手术标本病理证实有肠淋巴管扩张症;5)辅助检查证明肠道丢失蛋白质增多。具备前3条为疑诊,具备后2条即可确诊;排除继发性因素,可诊断原发性IL[1]。
确诊IL主要依据内镜活检或手术病理诊断。内镜直视下病变肠黏膜水肿、肥厚,表面附着奶黄色或雪片状突起(多发白色假性息肉),甚至肠狭窄;病理检查光镜下可见黏膜、黏膜下、浆膜层淋巴管扩张,肠绒毛末端膨大呈杵状,顶端出现破裂,但肠绒毛无萎缩表现。由于IL病变可弥漫或局限分布,累及肠管不连续,为保证病理结果准确性,往往多部位取材,这对于无法行胶囊内镜及肠镜检查的婴幼儿或病变位于内镜不能到达的肠管部位的患者,临床诊断存在困难。
有关肠蛋白丢失显像已于平台病例126号报道过,但该检查仅可判断肠道有无蛋白丢失,并不能对淋巴管发育情况作出判断。淋巴显像诊断IL特异性和阳性预测值均较高,对于临床疑诊IL的病例,淋巴显像更有助于明确诊断。其原理为:99mTc-DX经皮下注射后由淋巴系统转运,到达乳糜池,再经肠干逆流进入扩张的肠淋巴管,并随淋巴液(乳糜液)漏出至肠腔或腹腔,形成肠形放射性浓聚影,且随肠道的蠕动而移动。但该显像在部分患者可能会出现假阴性。影响显像结果的因素包括:(1)肠淋巴管扩张分布的部位,即位于肠壁的黏膜面还是浆膜面,前者漏出到肠腔,后者则可能漏出到腹腔;(2)淋巴液漏出量,病变累及范围小、淋巴管扩张程度轻,漏出量少,可能会出现假阴性结果[2]。而将肠蛋白丢失显像与淋巴显像联合,既能确定有无肠蛋白丢失,也能确定是否经肠淋巴管丢失,提高了对IL诊断的准确性。值得注意的是,由于漏出液在肠道内的移动、患者体位和机体状态等的变化,有时两种显像所提示病变部位并不一致。
关于IL的治疗,继发IL以去除病因为主,而对于PIL的患者,低脂、高蛋白、补充中链三酰甘油(MCT)的饮食治疗是其主要的治疗手段;而对于肠道的病变呈节段性或局灶分布的部分患者,在内科保守治疗无效后,可外科手术切除部分局灶病变及进行淋巴管静脉分流术。
本例患者主要临床表现为低蛋白血症、腹泻及水肿,结合实验室检查,临床怀疑IL引起的肠蛋白丢失性肠病。99mTc-HAS显像提示患者存在蛋白丢失性肠病的问题,但不能确定是否由IL引起的。随后患者行淋巴显像,不仅证实患者存在IL,而且提示胸导管出口梗阻。结合患者慢性病史,推断该患者是由于胸导管末端结构异常,造成胸导管梗阻,进而引起淋巴管内压力升高,而使淋巴回流不畅,淋巴液淤滞,导致肠淋巴管扩张及乳糜尿。患者之前虽然行左肾周围淋巴管剥脱术,使乳糜尿得到有效控制,但没有解决胸导管梗阻这一根源问题,进而导致之后腹泻加重,同时出现水肿的症状。患者之后行手术解除胸导管梗阻后,症状得到好转,随访至今未再复发。
参考文献
1.厉有名, 张冰凌. 小肠淋巴管扩张症的研究现状. 诊断学理论与实践, 2008, 7(1): 9~11.
2.文哲, 童冠圣, 刘勇,等. 淋巴显像诊断小肠淋巴管扩张症的腹部影像分型及价值. 中华核医学与分子影像杂志, 2014, 34(2): 116~120.