作者:北京大学第一医院核医学科 崔永刚 范岩
病史及检查目的:
患者女性,34岁,间断头痛2年,发现血压增高1年,最高140/100mmHg。实验室肾功检查指标正常,腹部超声示右肾小,结构欠清。肾动脉彩超示右肾动脉狭窄。为明确诊断,行卡托普利(Captopril,CAP)介入试验99mTc-DTPA肾动态显像(图1-4)。
检查方法:
患者检查前需停用血管紧张素转换酶抑制剂(Angiotensin-converting-enzyme inhibitor,ACEI)药物和血管紧张素II阻断剂5个服药周期;停利尿剂3天;检查当日停服所有降压药。
卡托普利介入试验采取二日法方案:第1日行基础肾动态显像,检查方法同常规(略)。第2日行卡托普利介入肾动态显像,卡托普利用量50mg,分别于服药前、服药后15min、30min、60min及显像结束后监测血压;介入显像检查当日空腹,口服卡托普利 30min后进半流食并饮水500ml,服药1h后进行肾动态显像,显像方法及图像处理同常规肾动态显像(略)。
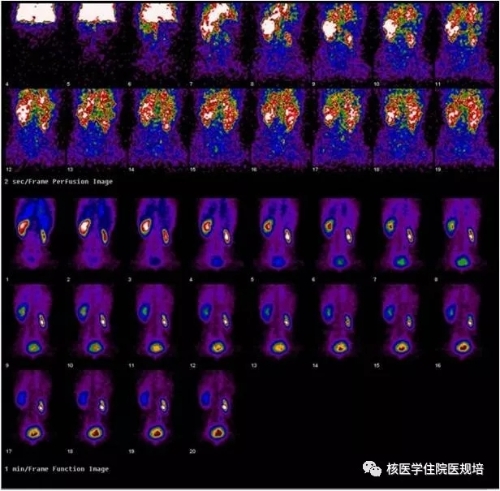
图1 基础肾动态显像
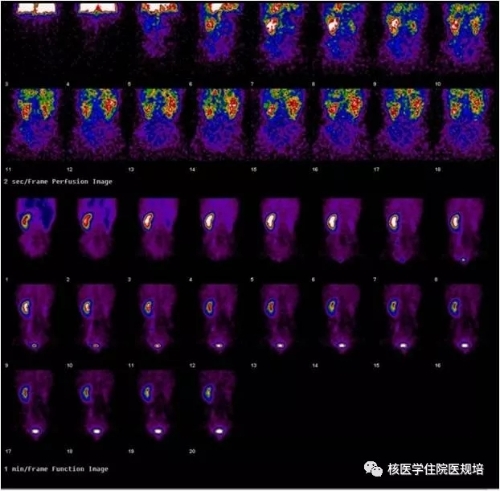
图2 卡托普利介入肾动态显像
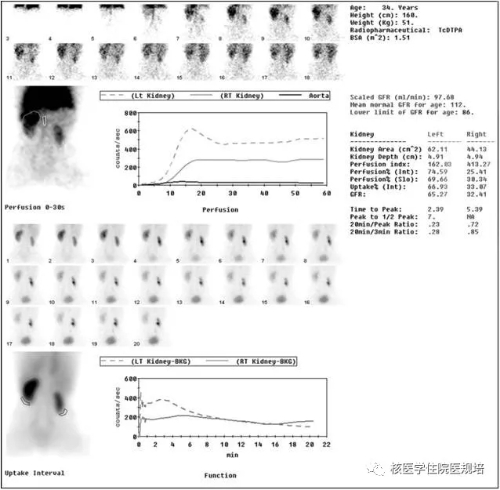
图3 基础肾动态显像-处理后图像、曲线及参数
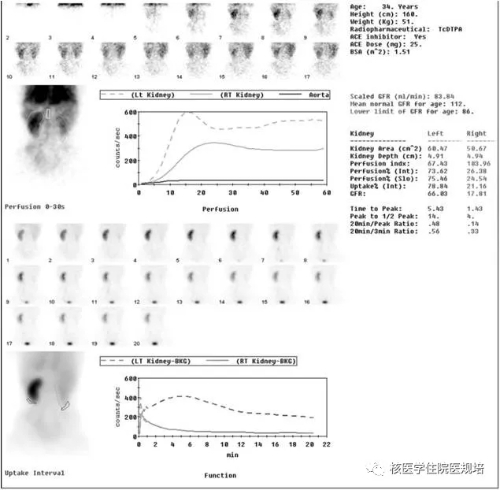
图4 卡托普利介入肾动态显像-处理后图像、曲线及参数
检查所见:
肾动脉灌注相:基础显像(图1),右肾影小,影像较淡;介入显像(图2),右肾显影极淡。基础及介入显像,左肾血流灌注影像正常。
肾功能相:基础显像(图1),右肾影像小,皮质清除显像剂速率减低;左肾大小和形态正常,皮质清除显像剂速率正常;至显像结束时,左肾盏肾盂内未见明显显像剂滞留;右肾盏肾盂内可见部分显像剂滞留。介入显像(图2),右肾影像极淡,轮廓不清,皮质清除显像剂明显减低;左肾皮质清除速率正常;至显像结束时,双侧肾盏肾盂内未见明显显像剂滞留。
肾图曲线:基础显像(图3),左肾图a、b、c段均正常;右肾图a段减低,b段上升斜率减低,c段下降缓慢;20分钟清除率:左肾72%,右肾15%。介入显像(图4),左肾图a段正常,b段上升斜率正常,峰时轻度后延,c段下降正常;右肾图a段低矮,未见b段,曲线呈低水平递减型;20分钟清除率:左肾52%,右肾67%(参考值≥40%)。
GFR值(ml/min):基础显像,左肾65,右肾33,总肾98;介入显像,左肾66,右肾 17,总肾 83(总肾参考值≥68)。
检查意见:
1、右肾小,血流灌注减低,功能受损,卡托普利介入试验阳性,考虑右侧肾动脉狭窄导致肾血管性高血压可能性大;
2、左肾血流灌注和功能正常,卡托普利介入试验阴性;
3、双侧上尿路引流通畅。
随访资料:
数字减影血管造影示:右肾动脉起始部狭窄90%,左肾动脉正常。患者随后行右肾动脉支架治疗,术后监测血压正常,考虑肾血管性高血压诊断明确。
病例相关知识及解析:
肾血管性高血压(Renal vascular hypertension,RVH)是继发性高血压中常见的类型之一,在美国人群发病率为3%~5%[1,2]。肾动脉狭窄(Renal arterystenosis,RAS)是引起RVH的常见原因,其产生RVH的主要机制是,肾动脉狭窄使肾脏血流灌注减低,激活肾素-血管紧张素-醛固酮系统(Renin-angiotensin aldosterone system,RAAS),造成外周血管收缩和水钠潴留,引起血流动力学改变,最终导致高血压。但不是所有肾动脉狭窄都可使RAAS激活继而引起高血压,虽然目前机制尚不明确,但多项研究发现临床上部分高血压患者存在与其血压增高无关的无血流动力学意义的单纯肾动脉狭窄[3]。因此,对于既有高血压又有肾动脉狭窄的患者,正确区别是RVH还是高血压合并单纯肾动脉狭窄很重要,因为两者治疗原则不同,前者经血管成形术能有效缓解高血压,而后者即使手术后也要终生服用降压药。
肾动脉狭窄诊断并不困难,X线肾动脉造影是金标准,超声能敏感探测血管狭窄程度及肾血流变化,常规肾动态也可间接反映肾动脉狭窄对肾功能造成的损伤。然而,对于合并有肾动脉狭窄的高血压患者,上述三种检查均不能提供肾动脉狭窄与高血压之间的关系。而卡托普利介入试验正是基于RVH患者存在由肾动脉狭窄引起的RAAS激活这一机制进行的,能有效协助RVH的诊断,并为进一步的有效治疗提供依据。
RVH患者肾动脉主干及其分支血管狭窄导致病侧肾血流灌注减少,刺激肾小球旁器使肾素分泌增多,进一步使血管紧张素II(AII)合成增多,AII使肾小球的出球小动脉收缩来维持肾小球内的滤过压,以保持正常的滤过分数和肾小球滤过率(GFR)。常规肾动态可表现为正常或轻微异常。卡托普利作为ACEI类药物,可阻止血管紧张素I(AI)转换成AII,其结果是使出球小动脉舒张,滤过压降低,GFR下降。这一机制使得卡托普利介入前、后的肾动态显像产生不同表现。典型表现是介入后肾动态显像显示患侧肾功能较介入前下降,皮质清除显像剂速率较介入前减低,一些相关的肾功能参数也会出现相应的变化,包括肾图曲线受损类型加重、分肾摄取率(Uptake ratio,UR)的下降、20分钟清除率(C20)的降低、峰时延长等。
卡托普利介入后引起的暂时性患肾功能降低表明肾动脉狭窄已造成肾脏低灌注及RAAS激活,是具有血流动力学意义的,可提示RVH的诊断。美国核医学协会肾血管性高血压的诊断指南指出:介入实验后患肾GFR下降≥10%,UR下降≥10%,单侧肾皮质较基础显像出现明显的显像剂清除延迟,均高度提示RVH;当患肾UR下降5%~9%时,提示RVH中度可能性[4]。作为功能性诊断RVH的方法,在临床高度怀疑继发性高血压的人群中,卡托普利介入试验的灵敏度和特异性可达到90%以上。
卡托普利介入试验除了作为无创性RVH辅助诊断方法以外,在肾血管重建术疗效预测方面的应用价值也已得到肯定。大量研究证实,术前卡托普利介入试验结果为阳性的患者,预示经皮肾血管成形术或外科手术治疗肾动脉狭窄后能有效控制高血压,对疗效阳性预测值可达92%;反之,结果为阴性则预示高血压治疗效果不好,外科手术获益有限,需谨慎评估或选择药物治疗方式。另外,利用此检查也有助于RVH患者选择抗高血压药物,结果阳性者提示ACEI治疗对患者肾功能可能会有影响,应在使用ACEI时密切监测肾功能。
卡托普利介入试验也有一定局限性,比如对双侧肾动脉狭窄、分支血管狭窄、肾功能受损严重者的诊断敏感性较低[5];若伴有上尿路梗阻时,准确性也会下降。另外,长期服用钙拮抗剂,也可能导致本检查的假阳性。
总的来说,卡托普利介入试验是一种安全有效的无创性检查方法,对于RVH的辅助诊断、治疗方案选择及预后判断方面有着重要的临床应用价值。
参考文献:
1.Setaro JF, Saddler MC, Chen CC, et al. Simplified captopril renography in diagnosis and treatment of renal artery stenosis. Hypertension, 1991, 18(3): 289-298.
2. Chonchol MB and Linas SL. Renalartery stenosis. Primary Care Case Review, 2002, 5(4): 167-173.
3.Elliott W J . Renovascular Hypertension: An Update[J]. Journal of clinical hypertension (Greenwich,Conn.), 2008, 10(7):522-533.
4.Taylor A T , Fletcher J W , Nally J V, et al. Procedure guideline for diagnosis of renovascular hypertension. Society of Nuclear Medicine[J]. Journal of Nuclear Medicine, 1998,39(7):1297-1302.
5.Chen CC, Hoffer PB, Vahjen G, et al. Patients at high risk for renal arterystenosis: a simple method of renal scintigraphic analysis with Tc-99m DTPA andcaptopril. Radiology, 1990, 176(2): 365-370.